Diferența dintre Carbocația și Carbanion | Carbocația vs Carbanion
Diferența cheie
între carbocație și carboanion este taxa lor; ele sunt ambele specii moleculare organice cu încărcături opuse. Carbocația este încărcată pozitiv cu ioni și carboanionul este ion încărcat negativ . Stabilitatea lor depinde de mai mulți factori, iar unele dintre ele sunt foarte importante în sinteza altor compuși chimici.
Ce este CarbocațiaCarbocația este o specie chimică care poartă o sarcină pozitivă pe un atom de carbon. Numele ei dă ideea clară că este un cation
(un ion pozitiv), iar cuvântul carbo se referă la un atom de carbon. Carbocalizarea include mai multe categorii; Carbocația primară, carbocația secundară și carbocația terțiară. Acestea sunt clasificate în funcție de numărul de grupări alchil atașate la atomul de carbon încărcat pozitiv. Stabilitatea și reactivitatea lor variază în funcție de acești substituenți. -> Carbonul este o specie moleculara organica cu o sarcina electrica negativa localizata pe un atom de carbon. Cu alte cuvinte, este un anion în care un atom de carbon posedă o pereche de electroni împărțită în comun cu trei substituenți. Numărul său total de electroni de valență este egal cu opt. Ele se formează prin eliminarea grupurilor încărcate pozitiv sau a atomilor dintr-o moleculă neutră. Ele sunt foarte importante ca intermediari chimici pentru a sintetiza alte substanțe, cum ar fi materialele plastice și polieten (sau polietilenă). Cel mai mic carbanoin este "ionul de metoxid" (CH 3
-
); format din metan (CH
4
) prin pierderea unui proton (H - ).

hibridă, iar p-orbitalul gol se află perpendicular pe planul a trei grupuri substituite. Prin urmare, are o structură moleculară planară trigonală. Carbocația necesită o pereche de electroni pentru a completa octetul. Aceștia pot reacționa cu nucleofili, pot fi deprotonați dintr-o legătură pi și pot avea rearanjamente la aceeași specie.
Carbanion:
Un carboanion alchil are trei perechi de legături și o singură pereche; astfel încât hibridizarea lui este sp 3, iar geometria este piramidală. Geometria alilului sau benzilcarboanionului este plană, iar hibridizarea este sp 2
. O octetul este complet în orbita cea mai exterioară a unui atom de carbon carboanionic și se comportă ca un nucleofil să reacționeze cu electrofilurile. Stabilitate: Carbocalizare: Stabilitatea carbohidrației depinde de diverși factori. Este mai stabil când mai multe grupuri -R sunt atașate la atomul de carbon pozitiv. Prin urmare, carbocarea terțiară este relativ stabilă decât cea primară. Structurile de rezonanță cresc, de asemenea, stabilitatea. Carbanion:
Stabilitatea carboanionului depinde de mai mulți factori; Electronegativitatea carbonului carbanionic, efectul de rezonanță, efectul inductiv cauzat de substituentul atașat și stabilizarea cu> grupările C = O, -NO2 și CN prezente pe carbonul carbanionic
Definiții: Efectul de inducție: Se poate observa efectul experimental transmiterea sarcinii printr-un lanț de atomi într-o moleculă, rezultând un dipol permanent într-o legătură.

Carbocarburant: Carbocitare primară:
Într-o carbocare primară (1 °), atomul de carbon încărcat pozitiv este atașat numai la o grupare alchil și la doi atomi de hidrogen.
Carbocitare secundară:
Într-o carbocare secundară (2 °), atomul de carbon încărcat pozitiv este atașat la alte două grupări alchil (care pot fi identice sau diferite) și un atom de hidrogen.
Carbocitare terțiară:
Într-o carbocare terțiară (3 °), atomul de carbon pozitiv este atașat la trei grupări alchil (care pot fi orice combinație de același sau diferit), dar fără atomi de hidrogen.
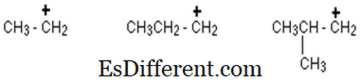
Carbanion:
Carboanionul este, de asemenea, clasificat în trei categorii în același mod ca și în carbocitare;

carboanion primar, carboanion secundar și carboanion terțiar
. Aceasta se face, de asemenea, pe baza numărului de grupări -R atașate la atomul de carbon anionic.

Referințe:
"Chimie. ": Carbanion. Accesat la 09 iunie 2016 de aici
"Carbocalizare. "Wikipedia. Accesat la 09 iunie 2016. de aici "Carbocații (sau ioni de carbon). "Chemguide. Accesat la 09 iunie 2016. de aici "Carbocații". Tutoriale chimice organice. Accesat la data de 09 iunie 2016. de aici

Datorită imaginii:
"Trendul de stabilitate a carbohidrației" de către Alatleephillips - Activitate proprie (CC BY-SA 4. 0) prin Wikimedia Carbanion Structural Formulas V - Activitate proprie (CC0) prin Wikimedia Commons


