Diferența dintre Thomson și Rutherford Modelul Atom | Thomson vs Rutherford Modelul Atom
Diferența cheie - Thomson vs. Rutherford Modelul atomului
Diferența cheie dintre modelul atomului Thomson și Rutherford este că modelul atomului Thomson nu conține detalii despre nucleu în timp ce modelul atomului Rutherford explică despre nucleul unui atom. J. J. Thomson a fost primul care a descoperit particula subatomică numită electron în 1904. Modelul propus de el a fost denumit "model de prune de prune al atomului". Dar în 1911, Ernest Rutherford a venit cu un nou model pentru atom după descoperirea nucleului atomic în 1909.
CUPRINS> 1. Prezentare generală și diferență cheie
2. Ce este Thomson Model de Atom
3. Ce este Rutherford Model de Atom
4. Comparație comparativă comparativă - Thomson vs. Rutherford Model de atom în formă tabulară
5. Rezumat
Ce este Thomson Model of Atom?
Modelul atomului Thomson este numit
modelul de budinca Plum , deoarece afirmă că atomul arată ca o budincă de prune. Singurele detalii cunoscute despre atom în acel moment au fost, -
Atomii sunt compuși din electroni- Electronii sunt particule încărcate negativ
- Atomii sunt încărcați în mod neutru
- Deoarece electronii sunt încărcați negativ, Thomson a sugerat că ar trebui să existe o taxă pozitivă pentru a neutralizează sarcina electrică a atomului. Modelul atomului Thomson explică faptul că electronii sunt încorporați într-un material solid încărcat pozitiv, care are o formă sferică. Această structură arată ca o budincă cu prune înglobate pe ea și a fost numită ca model de prune de prune de atom. Aceasta a dovedit ipoteza conform căreia un atom este încărcat neutru, deoarece acest model afirmă că încărcăturile negative ale electronilor sunt neutralizate de sarcina pozitivă a sferei solide. Deși acest model a demonstrat că atomii sunt încărcați în mod neutru, a fost respins după descoperirea nucleului.

Ce este modelul Rutherford al atomului?
Conform modelului de atom al lui Rutherford, așa-numitul model de budincă de prune de Thomson a fost incorect. Modelul de atom al lui Rutherford este de asemenea numit
modelul nuclear deoarece oferă detalii despre nucleul unui atom. Experimentul celebru numit "experimentul cu folie de aur Rutherford" a condus la descoperirea nucleului. În acest experiment, particulele alfa au fost bombardate printr-o folie de aur; se așteptau să treacă direct prin folia de aur. Dar, în loc de penetrare dreaptă, particulele alfa s-au transformat în direcții diferite.
Figura 02: Experimentul Foaie de aur Rutherford
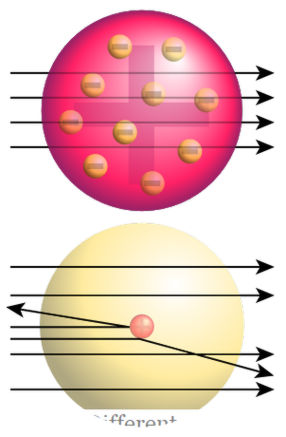
Sus: Rezultatele asteptate (Penetrarea drepta) Partea inferioara : Rezultatele observate cu o încărcătură pozitivă în folia de aur care provoacă o coliziune cu particule alfa. Rutherford a numit acest nucleu pozitiv ca nucleu. Apoi a sugerat modelul nuclear pentru atom; a fost compus dintr-un nucleu încărcat pozitiv și electroni încărcați negativ care înconjoară nucleul. El a sugerat, de asemenea, că electronii se află în orbitale în jurul nucleului la anumite distanțe. Acest model este de asemenea numit modelul planetar
deoarece Rutherford a sugerat că electronii sunt localizați în jurul nucleului, similar cu planetele situate în jurul soarelui. Conform acestui model, Atomul este compus dintr-un centru pozitiv încărcat care este numit nucleu. Acest centru conține masa atomului.
Electronii sunt situați în afara nucleului în orbitale la o distanță considerabilă.
- Numărul de electroni este egal cu numărul de încărcări pozitive (denumite mai târziu protoni) în nucleu.
- Volumul nucleului este neglijabil în comparație cu volumul atomului. Prin urmare, cea mai mare parte a spațiului din atom este goală.
- Totuși, acest model de atom al lui Rutherford a fost de asemenea respins, deoarece nu putea explica de ce electronii și încărcăturile pozitive din nucleu nu sunt atrase unul de celălalt.
- Figura 03: Modelul de atomi Rutherford
Care este diferența dintre Thomson și Rutherford Model Atom?

- diff Articolul Mijloc înainte de Tabel ->
Thomson vs. Rutherford Modelul atomului
Modelul atomului Thomson este modelul care afirmă că electronii sunt încorporați într-un material solid încărcat pozitiv, care are o formă sferică.
Modelul atomului Rutherford este modelul care explică faptul că există un nucleu în centrul atomului și că electronii sunt localizați în jurul nucleului. |
|
| Nucleus | Modelul atomului Thomson nu oferă detalii despre nucleu. |
| Modelul de atom al lui Rutherford oferă detalii despre nucleul unui atom și localizarea acestuia în interiorul atomului. | |
| Locația electronilor | Conform modelului atomului Thomson, electronii sunt încorporați într-un material solid. |
| Modelul lui Rutherford spune că electronii sunt localizați în jurul nucleului. | |
| Orbitale | Modelul atomului Thomson nu oferă detalii despre orbitale. |
| Modelul atomului Rutherford explică despre orbitale și că electronii sunt localizați în aceste orbite. | |
| Mass | Modelul atomului Thomson explică faptul că masa unui atom este masa solidului încărcat pozitiv, unde sunt încorporați electroni. |
| Conform modelului de atom al lui Rutherford, masa unui atom este concentrată în nucleul atomului. | |
| Rezumat - Thomson vs. Rutherford Modele de Atom | Modelele Thomson și Rutherford de atom au fost cele mai vechi modele pentru a explica structura unui atom. După descoperirea electronului de către J. J. Thomson, el a propus un model care să explice structura atomului. Mai târziu, Rutherford a descoperit nucleul și a introdus un nou model, folosind atât electron cât și nucleu. Principala diferență dintre modelul atomului Thomson și Rutherford este că modelul atomului Thomson nu conține detalii despre nucleu, în timp ce modelul atomului Rutherford explică nucleul atomului. |
Descărcați versiunea PDF a lui Thomson vs. Rutherford Modele de Atom
Puteți descărca versiunea PDF a acestui articol și o puteți utiliza în scopuri offline conform notei de citare. Vă rugăm să descărcați versiunea PDF aici Diferența dintre modelul Atoms Thomson și Rutherford.
Referință:
1. "Modelul Rutherford al atomului: Definiție și diagramă. "Studiu. com. n. d. Web. Disponibil aici. 06 iunie 2017.
2. Brescia, Frank. Fundamentele chimiei: o introducere modernă (1966). Elsevier, 2012. Imprimare.
3. Goldsby, Kenneth. Chimie. 12 ed. New York: McGraw-Hill, 2015. Imprimare.
Amabilitatea imaginii:
1. "Atom de prune de prune" (Domeniul Public) prin Wikimedia Wikimedia
2. "Atomul Rutherford" prin muncă proprie (CreateJODER Xd Xd) (CC BY-SA 3. 0) prin Wikimedia Commons
3. "Rezultatele experimentului cu folie de aur Rutherford" Utilizator: Fastfission Activitate proprie (Public Domain) prin Wikimedia Wikimedia




